EN tørcelle Batteriet blev opfundet i Japan under Meiji-æraen i 1887. I modsætning til vådcellebatterier bruger et tørcellebatteri en pastaformet elektrolyt med kun nok fugt til at tillade strøm at flyde. Det kan fungere i enhver retning uden at spilde, da det ikke indeholder fri væske, så det er velegnet til bærbart udstyr.
I dagens energibesparende verden er tørcellebatterier en af mange typer elektrokemiske celler, der er tilgængelige til forbrugerbrug, men det var en stor innovation, da det blev opfundet.
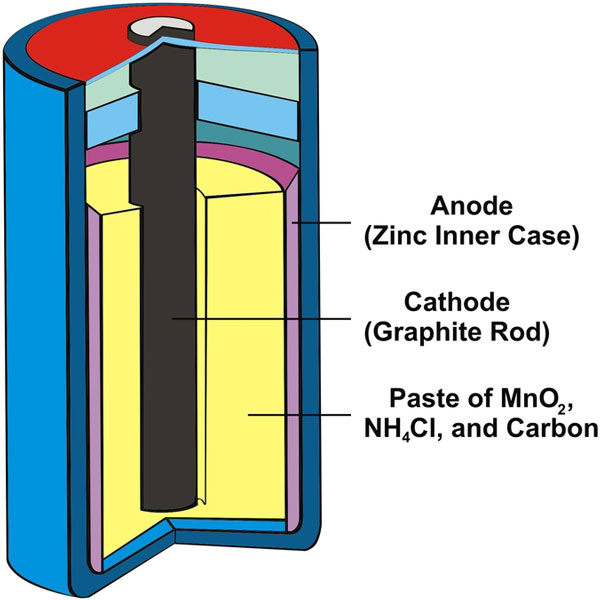

Et almindeligt tørcellebatteri er zink-kulstofbatteriet, som er en tilpasning af et vådcellebatteri, der kaldes Leclanché-cellen. Som du kan se på ovenstående illustration, består cellen af et zinkkamrer, der fungerer som anode. Katoden er en kulstofstang, der er fuldstændig omgivet af en pasta af kulstof, ammoniumchlorid (NH4Cl) og manganoxid (MnO2).
Batteriproducenter klassificerer batterityper som enten primære (engangsbatterier) eller sekundære (genopladelige). Tørre celler kan være enten primære eller sekundære celler.
Mindre tørcellebatterier, såsom alkaliske eller lithium-ion-batterier, bruges typisk i bærbar elektronik, såsom legetøj, telefoner og bærbare computere.
Fordele ved tørcelle
Da tørcellebatterier først blev udviklet, havde de mange fordele i forhold til vådcellebatterier. De første vådcellebatterier var ofte meget sarte og kunne lække fra deres kaustiske elektrolytter, når de blev vendt på hovedet eller simpelthen blev bevæget for kraftigt. Tørcellebatterier var meget mindre flygtige og kunne overleve meget hårdere behandling. I moderne tid gelbatterier har løst de fleste af de værste problemer med vådcellebatterier, men tørcellebatterier har stadig fordele i visse anvendelser.
Hvad er forskellen mellem tørcelle og vådcelle


